علاج الثعلبة AGA : التطورات في العلاج البيولوجي للثعلبة الأندروجينية
علاج الثعلبة AGA أصبح موضوعًا مثيرًا للاهتمام في مجال الطب الحديث، حيث يسعى العلماء والأطباء لتطوير حلول فعالة لمشكلة تساقط الشعر الأندروجيني. تعتبر الثعلبة الأندروجينية من أكثر أنواع تساقط الشعر شيوعًا، وتؤثر على ملايين الأشخاص حول العالم، مما يسبب لهم قلقًا نفسيًا واهتمامًا متزايدًا بالعلاجات المتاحة.
في هذا المقال، سنستعرض أحدث التطورات في العلاج البيولوجي للثعلبة الأندروجينية. حيث يتم استكشاف العلاجات المستندة إلى التكنولوجيا الحيوية وكيف يمكن أن تحدث ثورة في طريقة معالجة هذه الحالة. سنناقش العقاقير الجديدة، وآليات العمل، والتجارب السريرية التي تُظهر فاعلية هذه العلاجات. انضم إلينا في استكشاف هذا المجال المتقدم، واستعد للاطلاع على الأمل الجديد في استعادة الشعر والثقة بالنفس.
جدول المحتويات
ماهو داء الثعلبة ؟
تعتبر حالة تساقط الشعر الوراثي، المعروفة محلياً باسم “داء الثعلبة” (Androgenetic Alopecia – AGA) وعلمياً باسم “الصلع الذكوري الأنثوي”. وهو من أكثر أنواع تساقط الشعر شيوعاً، حيث تؤدي إلى تصغير بصيلات الشعر وتناقص كثافته بشكل تدريجي. تصيب هذه الحالة كل من الرجال والنساء، لكن الرجال هم الأكثر تأثراً بها. تشير الدراسات إلى أن نسبة انتشار AGA تصل إلى 21.3%، وتزداد هذه النسبة مع تقدم العمر. من المهم فهم أن هذا النوع من تساقط الشعر ليس له تأثيرات جسدية فحسب، بل ينعكس أيضاً على الصحة النفسية للمصابين، مما يؤدي إلى انخفاض الثقة بالنفس والشعور بالقلق.
نظرًا للتأثيرات السلبية التي تحدثها AGA على المظهر الشخصي والصحة النفسية، فإن البحث عن طرق علاج فعالة لهذه الحالة يُعتبر ذا أهمية كبيرة. تتنوع خيارات العلاج بين الأدوية مثل المينوكسيديل وفيناسترايد، والعلاجات الطبيعية مثل زيت الخروع والفيتامينات. بالإضافة إلى ذلك، قد يلجأ البعض إلى التقنيات الحديثة مثل زراعة الشعر أو العلاج بالليزر. من الضروري استشارة مختص في الأمراض الجلدية لتحديد أنسب خيارات العلاج بناءً على الحالة الفردية.
مسببات الصلع الوراثي (AGA) وحالة العلاج
تشير الأبحاث الحديثة إلى أن العوامل الوراثية والهرمونات الذكرية (الأندروجينات) هما السبب الأساسي في الإصابة بالصلع الوراثي.
- أظهرت الدراسات أن وجود طفرات في الجينات AR/EDA2R على الكروموسوم X والموقع 20p11 على الكروموسوم 20 يُعد من أهم العوامل الجينية المسببة.
- يعمل إنزيم 5-ألفا ريدكتاز على تحويل هرمون التستوستيرون إلى ديهدروتستوستيرون (DHT) داخل بصيلات الشعر. هذا الهرمون يمتلك قدرة أكبر على الارتباط بمستقبلات الأندروجين مقارنة بالتستوستيرون.
- وُجد أن مستوى إنزيم 5-ألفا ريدكتاز ومستقبلات الأندروجين أعلى بكثير في بصيلات المناطق المصابة بالصلع مقارنة بالمناطق السليمة، مما يؤدي إلى:
- قصر فترة نمو الشعر (Anagen phase).
- زيادة عدد بصيلات الشعر في مرحلة الراحة (Telogen).
- تقلص حجم البصيلات تدريجياً حتى تنتج شعراً أرق وأقصر (الشكل 1).
كما أن بعض الاختلالات الهرمونية والفيتامينية (مثل هرمونات الغدة الدرقية، الإستروجين، فيتامين A، فيتامين E) قد تلعب دوراً إضافياً في تطور المرض.
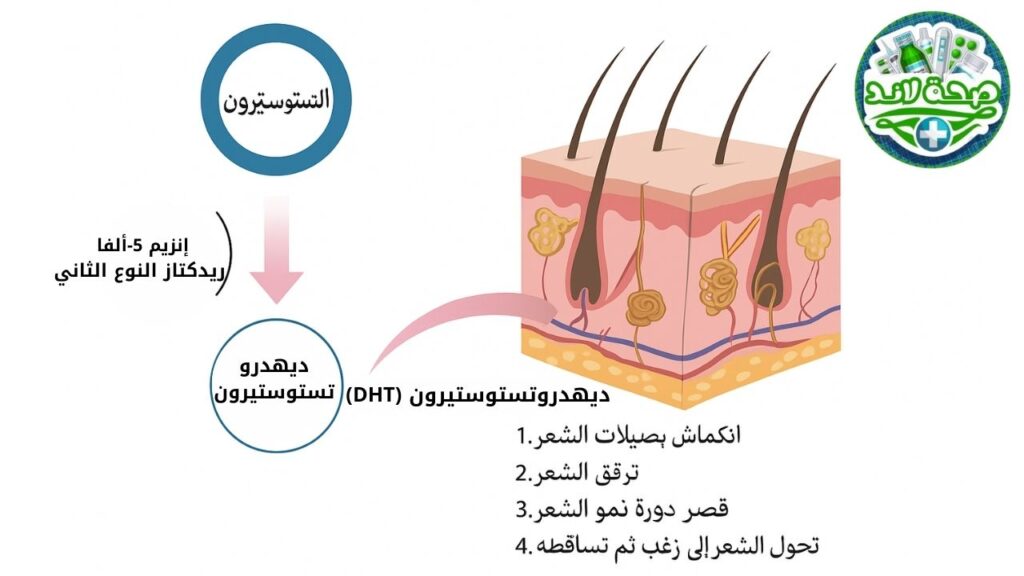
آلية تطور تساقط الشعر الوراثي داء الثعلبة (AGA)
تشير الأبحاث الحالية إلى أن العوامل الوراثية والهرمونية تعد من العوامل الرئيسية في ظهور تساقط الشعر الوراثي (AGA). فقد تم تحديد مواقع جينية معينة تعتبر نقاط خطر وراثية، مثل الطفرة في موقع AR/EDA2R على الكروموسوم X والموقع 20p11 على الكروموسوم 20. تلعب إنزيمات 5-α ريدوكتاز دورًا محوريًا في هذه العملية، حيث تقوم بتحويل التستوستيرون إلى ثنائي هيدروتستوستيرون (DHT). الذي يتمتع بقدرة أعلى على الارتباط بمستقبلات الأندروجين. كذلك أظهرت الدراسات أن مستويات التعبير عن 5-α ريدوكتاز ومستقبلات الأندروجين في منطقة تساقط الشعر أعلى من تلك الموجودة في المناطق غير المتأثرة. مما يؤدي إلى تقصير فترة النمو لبصيلات الشعر وزيادة عدد البصيلات في مرحلة الراحة، وبالتالي تسهم في تصغير حجم البصيلات.
الوضع الحالي لعلاج الثعلبة
بالنظر إلى التعقيدات المرتبطة بتطور داء الثعلبة، تتنوع خيارات العلاج المتاحة حاليًا. تشمل العلاجات الشائعة المينوكسيديل وفيناسترايد، حيث يعمل الأول على تحفيز نمو الشعر، بينما يثبط الثاني تأثير DHT. بالإضافة إلى ذلك، هناك اهتمام متزايد بالعلاجات الطبيعية مثل الفيتامينات (مثل فيتامين A وE) والهرمونات مثل هرمونات الغدة الدرقية والاستروجين، التي تلعب دورًا في تنظيم تقدم الحالة. من المهم أن يتم تقييم كل مريض بشكل فردي لتحديد العلاجات الأنسب، ما يستدعي استشارة متخصص في الأمراض الجلدية.
العلاجات التقليدية المعترف بها لـعلاج الثعلبة
تتضمن الخيارات العلاجية الحالية:
- الأدوية:
- مينوكسيديل موضعي بتركيز 2% أو 5%.
- فيناسترايد فموي.
القيود: بداية متأخرة لظهور النتائج، عودة تساقط الشعر بعد التوقف، آثار جانبية (صداع، ضعف جنسي، التهاب جلدي).
- العلاج بالليزر منخفض الطاقة: يساعد على تحسين الدورة الدموية وتحفيز البصيلات.
- زراعة الشعر: تعد خياراً جراحياً فعالاً لكنه لا يحل المشكلة جذرياً، إذ يعتمد على إعادة توزيع الشعر من منطقة إلى أخرى. القيود: محدودية عدد البصيلات المتاحة، مع مضاعفات محتملة مثل التندب، الالتهاب، الألم، أو تجمع الدم تحت الجلد.
الحاجة إلى علاجات جديدة
نظراً للقيود والآثار الجانبية المرتبطة بالعلاجات التقليدية، كذلك هناك حاجة ملحة لتطوير طرق علاجية أكثر فعالية وأماناً.
العلاج البيولوجي: الاتجاه الحديث
- يشمل كل العلاجات التي تعتمد على الجزيئات الحيوية الكبيرة مثل:
- العلاج الخلوي.
- العلاجات غير الخلوية (الأجسام المضادة، لقاحات البروتين أو الببتيد، اللقاحات الجينية، والعلاج الجيني).
- يستخدم العلاج البيولوجي بالفعل في علاج أمراض متعددة مثل:
- أمراض الجهاز الهضمي.
- الأمراض الجلدية.
- أمراض الدم.
- أمراض الكلى المستعصية.
- في السنوات الأخيرة: أظهرت الدراسات أن العلاج البيولوجي يحقق نتائج ملموسة في تحفيز تجديد الشعر مع آثار جانبية محدودة مقارنة بالطرق التقليدية.
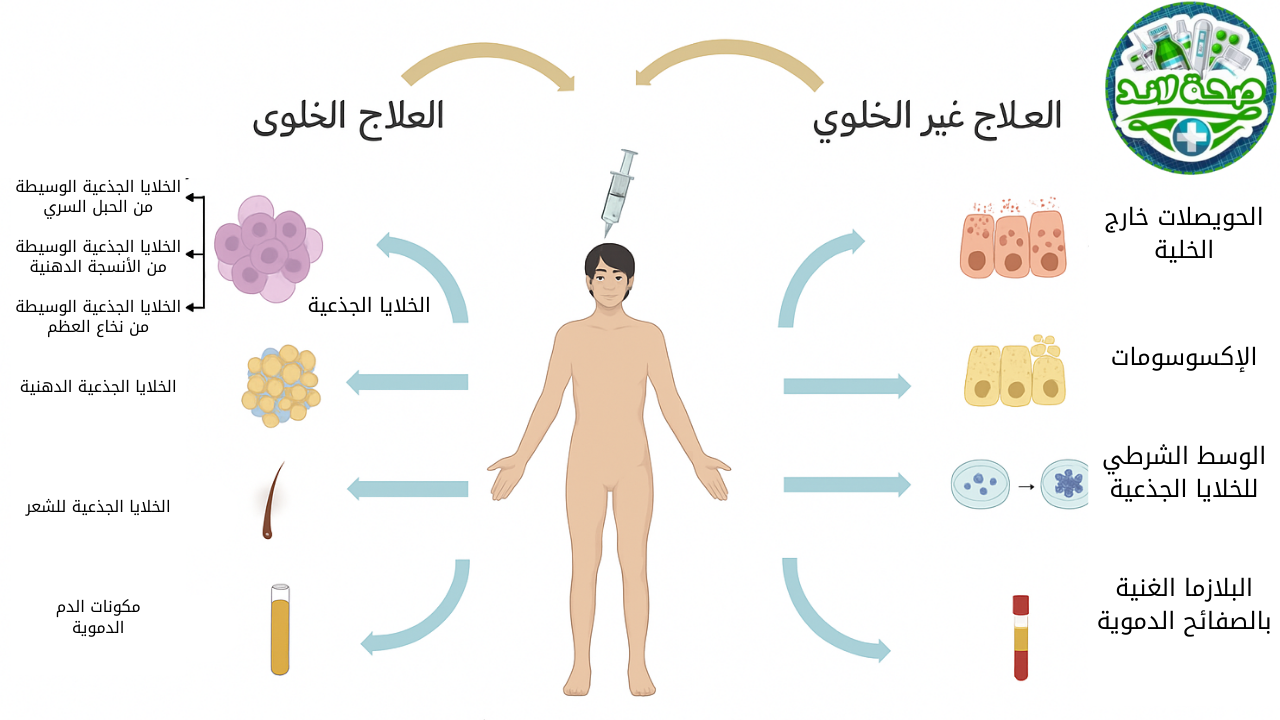
علاج داء الثعلبة بالخلايا
يتضمن العلاج الخلوي استخدام أساليب الهندسة الحيوية للحصول على خلايا ذات وظائف محددة. ومن خلال التوسع المختبري وعمليات الزراعة المتخصصة، كما تمنح هذه الخلايا القدرة على تعزيز المناعة والقضاء على مسببات الأمراض والخلايا السرطانية، وبالتالي علاج مرض محدد. وقد أظهرت الدراسات أن العلاج الخلوي لتساقط الشعر يمكن أن يعزز تجديد أو إصلاح أنسجة مثل الشعر.
خلايا الجذع الوسيطة ودورها في علاج الثعلبة
تعتبر خلايا الجذع الوسيطة (MSCs) نوعًا من الخلايا الجذعية متعددة القدرات، التي تمتلك القدرة على التجدد الذاتي والتمايز إلى أنواع مختلفة من الخلايا مثل الغضاريف، والعظام، والدهون، والعضلات القلبية، والأعصاب. توجد هذه الخلايا في عدة أنسجة وأعضاء، بما في ذلك الدهون، ونخاع العظم، والجلد، والحبل السري، والكبد، والرئتين. كما تلعب MSCs دورًا مهمًا في الحفاظ على استقرار الأنسجة والأعضاء من خلال تنظيم المناعة، وتعزيز تكوين الأوعية الدموية، ومكافحة موت الخلايا. وقد أظهرت الدراسات أن MSCs المستمدة من مصادر مختلفة تتمتع بقدرة على تعزيز نمو الشعر.
مصادر خلايا الجذع الوسيطة وتطبيقاتها
تعتبر خلايا الجذع الوسيطة المستمدة من الحبل السري (UCB-MSCs) نوعًا من الخلايا الجذعية الموجودة في أنسجة الحبل السري للمولود الجديد. كما تظهر الأبحاث أن هذه الخلايا تفرز عوامل نمو مثل بروتين ربط عامل النمو الشبيه بالأنسولين-1 (IGFBP-1) وعامل نمو البطانة الوعائية (VEGF) بطريقة مجاورة، مما يسرع من نمو بصيلات الشعر. في الدراسات، أظهرت حقن UCB-MSCs في نموذج تدهور بصيلات الشعر لدى الفئران فعالية كبيرة في منع تدهور البصيلات.
أما خلايا الجذع الوسيطة المستمدة من الدهون (AD-MSCs)، فهي خلايا جذعية تستخرج من الأنسجة الدهنية ولها خصائص مشابهة لـ MSCs. كذلك يعتقد أن AD-MSCs تعمل على علاج تساقط الشعر من خلال تفرز عوامل نمو مثل VEGF، وعوامل نمو الكبد (HGF)، وعوامل نمو الصفائح الدموية (PDGF)، مما ينشط دورة نمو الشعر. كما تسهم هذه الخلايا في تحسين تدفق الدم إلى بصيلات الشعر من خلال إفراز سيالات مثل البروستاجلاندين E2، مما يعزز من تغذية الخلايا الشعرية.
في الدراسات السريرية، تم استخدام MSCs لعلاج 50 مريضًا مصابًا بتساقط الشعر الوراثي. حيث أظهرت النتائج زيادة في عدد الشعر وقطر الشعيرات في المجموعة المعالجة. كما أظهرت دراسة أخرى أن حقن خلايا الجذع الوسيطة المستمدة من نخاع العظم (BM-MSCs) أدى إلى زيادة ملحوظة في كثافة الشعر وسرعة نموه. تعتبر AD-MSCs خيارًا مفضلًا نظرًا لسهولة جمعها وكفاءتها العالية. بينما تتمتع UCB-MSCs بقدرة أعلى على التكاثر ومجموعة أوسع من إمكانيات التمايز.
خلايا الجذع المستمدة من الدهون ودورها في علاج الثعلبة
تعتبر خلايا الجذع المستمدة من الدهون (ADSCs) نوعًا من الخلايا الجذعية التي تستخرج من أنسجة الدهون في الجسم، وتمتاز بقدرتها على التجدد والتمايز. تشبه ADSCs خلايا الجذع الوسيطة (AD-MSCs) في الخصائص والوظائف. لكن AD-MSCs تعتبر جزءًا من مجموعة خلايا الجذع الوسيطة وتتطلب إجراءات أكثر تعقيدًا لاستخراجها. أظهرت الأبحاث أن ADSCs تنتج وتفرز عوامل نمو مثل VEGF وHGF وIGF-1. مما يساعد في تنظيم بيئة بصيلات الشعر وتعزيز نموها من خلال خصائصها المضادة للالتهابات والأكسدة.
تطبيقات خلايا الجذع في علاج تساقط الشعر
أظهرت الدراسات السريرية أن حقن ADSCs في فروة الرأس لدى النساء المصابات بتساقط الشعر يؤدي إلى تقليل الالتهاب وزيادة كثافة الشعر وقطر الشعيرات. تمثل ADSCs خيارًا مثاليًا لعلاج تساقط الشعر نظرًا لسهولة جمعها وكفاءتها العالية، مما يجعلها علاجًا واعدًا لتساقط الشعر الوراثي.
خلايا الجذع من بصيلات الشعر وتطبيقاتها
تعتبر خلايا الجذع من بصيلات الشعر (HFSCs) خيارًا آخر لعلاج تساقط الشعر. يتم استخراج HFSCs من بصيلات الشعر وزراعتها قبل إعادة حقنها في مناطق تساقط الشعر. أظهرت الدراسات أن استخدام HFSCs يمكن أن يزيد من كثافة الشعر بنسبة ملحوظة. رغم ذلك، لا تزال فعالية HFSCs ووسائل استخدامها بحاجة إلى مزيد من البحث لتقييم أمانها ونتائجها.
مكونات الأوعية الدموية ودورها في تعزيز نمو الشعر
تشير مكونات الأوعية الدموية (SVF) إلى مجموعة من الخلايا المتنوعة التي تستخرج من الدهون، بما في ذلك ADSCs. تتميز SVF بسهولة تحضيرها مقارنةً بـ AD-MSCs، وتظهر خصائص مضادة للالتهابات وتعزز نمو الشعر. كما أظهرت دراسات أن حقن SVF يسهم في زيادة كثافة الشعر، وتفوقت SVF على العلاجات الأخرى مثل البلازما الغنية بالصفائح الدموية (PRP).
خلايا الجذع متعددة القدرات المستحثة
تعتبر خلايا الجذع متعددة القدرات المستحثة (iPSCs) نوعًا مبتكرًا من الخلايا الجذعية التي تم تطويرها عن طريق إعادة برمجة خلايا الجسم. كما أظهرت الأبحاث أن iPSCs يمكن أن تتمايز إلى خلايا بديلة لبصيلات الشعر، مما يشير إلى إمكانية استخدامها لعلاج تساقط الشعر. ومع ذلك، لا تزال الأبحاث في هذا المجال مقيدة بالاعتبارات الأخلاقية وسلامة الاستخدام في البشر.
علاج داء الثعلبة بدون خلايا
تقنيات العلاج غير الخلوي هي علاجات طبية تجديدية غير خلوية قائمة على الخلايا. وتشمل بشكل رئيسي مشتقات الخلايا الجذعية الوسيطة (MSC)، والحويصلات الخلوية، والإكسوسومات. تتكون مشتقات الخلايا الجذعية الوسيطة من مجموعة متنوعة من المواد النشطة بيولوجيًا. بما في ذلك عوامل النمو، والسيتوكينات، والأحماض النووية، وعوامل غذائية أخرى، والتي تلعب دورًا حاسمًا في تنظيم دورة نمو بصيلات الشعر وتجديد الشعر. كذلك تتكون مشتقات الخلايا الجذعية الوسيطة بشكل رئيسي من حويصلات خارج الخلية وعوامل قابلة للذوبان في وسط مكيف.
1. الحويصلات الخلوية
الحويصلات هي تراكيب صغيرة مكوّنة من غشاء مزدوج، وتقسم حسب حجمها إلى:
- أجسام موت الخلية (>1000 نانومتر)
- الحويصلات الدقيقة (100–1000 نانومتر)
- الإكسوسومات أو الحويصلات خارج الخلية (30–150 نانومتر)
تحتوي هذه الحويصلات على بروتينات، أحماض نووية (mRNA وmiRNA وغيرها)، جزيئات لاصقة، دهون، وعوامل نمو. وقد تبين أن بعض هذه المحتويات مثل الـ miRNA وmRNA والبروتينات لها دور في ترميم الأنسجة وتجديدها.
كما أثبتت الدراسات أن الحويصلات تحمل أكثر من 20 نوعاً من عوامل النمو المرتبطة بإنبات الشعر مثل HGF وEGF وVEGF وb-FGF التي تحفّز نمو الشعر، في حين أن عامل TGF-β يثبط نمو بصيلات الشعر.
تجارب على الحيوانات أظهرت أن حقن هذه الحويصلات المشتقة من الخلايا العصبية أو الخلايا الدهنية أو الجلدية يؤدي إلى زيادة تكاثر خلايا بصيلات الشعر وتحفيز نموها. كما أظهرت دراسة سريرية أن جلسة واحدة من العلاج بهذه الحويصلات عند مرضى الصلع الوراثي حسّنت كثافة الشعر بعد 6 أشهر دون ظهور آثار جانبية تُذكر.
2. الإكسوسومات (Exosomes)
الإكسوسومات هي نوع من الحويصلات خارج الخلية، حجمها بين 30–150 نانومتر، وتفرزها معظم أنواع الخلايا مثل الخلايا الجذعية، الدهنية، المناعية والصفائح الدموية.
تعمل هذه الإكسوسومات كرسائل بيولوجية، حيث تحمل بروتينات ودهون وأحماض نووية وتتفاعل مع الخلايا المستهدفة بطرق متعددة، مما يمنحها دوراً في:
- ترميم الأنسجة
- تنظيم المناعة
- تقليل الالتهاب والإجهاد التأكسدي
الأبحاث أظهرت أن الإكسوسومات المشتقة من الخلايا الجذعية قادرة على تنشيط بصيلات الشعر الخاملة وتحفيز نموها من خلال:
- تنظيم بعض الـ miRNA وتنشيط مسار Wnt/β-catenin، مما يمنع موت الخلايا ويشجع على النمو.
- تعزيز دخول بروتين β-catenin إلى النواة مما يزيد من تجديد البصيلات.
- مقاومة تأثير هرمون DHT المسبب لتساقط الشعر عن طريق تعطيل مسار TGF-β/SMAD3.
كذلك، الإكسوسومات المشتقة من خلايا الحلمة الجلدية (Dermal Papilla Cells) تحتوي على جزيئات مثل miR-218-5p وmiR-22-5p التي تساعد على نمو وتطور البصيلات عبر تنشيط مسار Wnt/β-catenin. ورغم النتائج الواعدة، إلا أن الأمان طويل المدى لهذا العلاج لا يزال بحاجة لمزيد من الدراسات.
3. الوسط المكيف بالخلايا الجذعية (Conditioned Medium)
هو سائل خاص تزرع فيه الخلايا الجذعية في بيئة معينة فتفرز عوامل نمو تذوب فيه، وهذه العوامل تساعد على تحفيز البصيلات.
على سبيل المثال: في ظروف نقص الأكسجين، تفرز الخلايا الجذعية عوامل مثل KGF وVEGF وb-FGF التي تساهم في نمو الشعر.
دراسات سريرية:
- عند حقن الوسط المكيف المشتق من الخلايا الجذعية الدهنية (ADSCs) في فروة مرضى الصلع الوراثي مرة شهرياً لستة أشهر، لوحظت زيادة في كثافة الشعر وعدد البصيلات في طور النمو.
- أبحاث أخرى باستخدام وسط مكيّف من خلايا دم الحبل السري (UCB-MSCs) أو نخاع العظم (BM-MSCs) أظهرت نتائج مشابهة بتحسين الكثافة وسماكة الشعرة.
لكن ما يزال الحصول على هذه الأوساط من بعض المصادر (مثل نخاع العظم والحبل السري) محدود، وآليات عملها على المدى البعيد تحتاج لدراسات إضافية.
4. البلازما الغنية بالصفائح (PRP)
البلازما الغنية بالصفائح هي منتج يُستخلص من دم المريض نفسه بعد معالجته بالطرد المركزي، وتحتوي على:
- صفائح دموية تطلق عوامل نمو (VEGF، EGF، IGF، FGF وغيرها)
- كريات بيضاء تعمل كمضاد للعدوى
- الفيبرين الذي يوفّر دعامة للخلايا
هذه العوامل تلعب دوراً في تنشيط بصيلات الشعر. الدراسات أوضحت أن:
- PRP يحفّز دخول البصيلات في مرحلة النمو (Anagen) عبر تنشيط مسارات Wnt/β-catenin وERK وAkt.
- يعزز كثافة الشعر وسماكته، مع فاعلية أكبر عند الرجال مقارنة بالنساء.
- دمجه مع علاجات أخرى مثل المينوكسيديل أو الخلايا الجذعية يزيد من فعاليته.
لكن من الملاحظ أن نتائج العلاج بـ PRP قد تختلف من شخص لآخر، ليس بسبب عدد الصفائح أو تركيز عوامل النمو فقط، بل بسبب التوازن فيما بينها.
اقرا ايضا : أفضل 10 منتجات طبيعية للعناية بالشعر الجاف (استعد لشعر أكثر نعومة)
الخلاصة
تشير مراجعة الأبحاث إلى أن العلاجات البيولوجية (علاج الثعلبة) مثل:
- الخلايا الجذعية (MSCs، ADSCs، HFSCs)
- الوسط المكيف بالخلايا الجذعية
- الحويصلات والإكسوسومات
- البلازما الغنية بالصفائح (PRP)
قد تُساهم بشكل ملحوظ في زيادة كثافة وقطر الشعر لدى مرضى الصلع الوراثي (AGA). وهذا يجعل العلاج البيولوجي خياراً واعداً في هذا المجال.
لكن ما زالت هناك تحديات قائمة:
- معظم الدراسات صغيرة وعلى نطاق محدود، لذلك تحتاج الأدلة إلى تعزيز من خلال أبحاث أكبر ومتعددة المراكز.
- سلامة العلاج بالخلايا الجذعية على المدى الطويل لم تدرس بشكل كافٍ، مما يحد من استخدامه.
- لم يحدد بعد ما إذا كان العلاج البيولوجي مناسباً لكل مريض بالصلع الوراثي، وما هي المؤشرات المثلى لاستخدامه.
- فعالية الدمج بين العلاج البيولوجي والعلاجات التقليدية (مثل المينوكسيديل أو الأدوية الأخرى) ما زالت بحاجة لدراسة أوسع.
النتيجة: الاستخدام المنظم والآمن للعلاج البيولوجي قد يفتح طرقاً جديدة وأكثر فعالية لعلاج الصلع الوراثي.




